湖南优质导尿回流袋批发
发布时间:2023-03-18 00:39:26
湖南优质导尿回流袋批发
更重要的是,随着行业发展,医疗器械的经销商们已经在不知不觉间成为强势的一方,对生产商有了话语权。 医疗器械销售这一行是典型的“赢者通吃”,市场、渠道、关键性人物就那么几个(主要是当地联采办、三甲医院院长等),且不具备可替代性,因而医疗器械行业两类人具有优势:先发者,或者关系大户。 而地区的大经销商,基本上两类都是,早些年医疗器械跨国药企大举进入中国时,招聘总监级别的岗位时,没点政府背景都入不了他们的法眼。而这些老玩家们多年深耕经营,不仅积累了大量人脉和经验,也基本掌握了地区大部分的医疗器械代理渠道。 因此,即使新进入市场的企业有直销的念头,也很难突破藩篱、承担成本,终往往还是投向了经销商的怀抱。 这是另一层面上的垄断——经销商对销售渠道的垄断。技术壁垒和流通渠道,兜兜转转,价格虚高始终离不开“垄断”二字。 那么,如何才能让医疗器械的价格降下来? 如前文所述,医疗器械的高价格分为生产和流通两个部分。前者囿于海外药企的技术垄断所导致的高定价,下游自然没有话语权;而另一边,代理商们又可以仗着渠道优势肆无忌惮的加价。 医疗器械的高定价需要引入足够的玩家来用市场化机制破除;而集采大背景下,药品直接打包给医院,经销商可能会随着加价空间的消失,而逐渐退出历史舞台。 也就是说,集采既能够打破外企高价垄断,又能压缩经销商的多级抬价。这是近几年医改探索出来的控费之路,也要逐渐应用在医疗器械领域,而这一切的前提,就是细分领域有足够多的竞争玩家。 讲道理,进口医疗器械受限于本国高昂的研发、审批、劳动力和运输等成本,而国内企业基于模仿,研发、人力、原材料成本都相对低廉,又受到政策倾斜照顾,在成本方面具有不可比拟的优势。 然而现实情况是,因为起步时间晚,很多国产器械只能走低端化路线,但质量始终没能迎头赶上。所以,近几年国内医疗器械市场规模在不断扩大,而不良反应报告也逐年增多,直到2019年才有所好转。 这种情况下,消费者的选择也很真实。虽然国产设备厂商很愿意与医院方多做交流,在设备使用中,会根据院方的意见,在性能和设计上做进一步完善,遇到什么问题,会及时解决,医生操作起来更顺手;然而,当医院做一些科研或教学任务时,仍然会使用进口设备。 而另一种情况是,很多国产器械在走汽车行业的老路:不少国产CT机虽然是自己的,但其中诸如CT探测器(相当于照相机的感光元件)、信号链(处理图像的专用芯片模块)仍然绕不过前面提到的GPS三巨头。 国内的医疗器械虽然通过“连抄带借”完成了一部分自主化,但这终究只是企业短期生存的需要,而这种精细制造业是一个长期积累的过程,这二者之间的矛盾让本土的医疗器械直到如今也没能走出“低端制造”的怪圈。 我国医疗器械公司呈现小、散、乱、多的局面,我国有超过18000家医疗器械企业,其中90%以上规模在2000万元以下。 早在2015年,“生物医药及高性能医疗器械”就被列入《中国制造2025》,成为重点突破发展的十大领域之一,与信息技术、航空航天等核心产业并驾齐驱。 中美贸易摩擦开始后,特朗普用几道禁令轻而易举地掐住了华为、中兴的喉咙。从那时起,“自主可控”有一次成了我国高科技产业的一个执念。谈论多的当然是半导体。不过,疫情冲击下,也有越来越多人开始意识到在医药领域自主崛起的重要性。 如果说半导体行业关乎人的发展,那么医药行业关乎的是人的生存。民众被“看病难”“看病贵”“天价进口药”“天价手术”折磨的那些年,是时候成为历史了。 在药品领域,全国性集采已经常态化,在药品领域,当年的“神药”和“仿制药大户”已经逐渐在向创新药企的转型。而在“脱钩”之声此起彼伏的当下,IVD、彩超、CT、手术机器人等器械领域的突破自然也刻不容缓。中国高科技产业的攻坚,不能只有一个华为。

湖南优质导尿回流袋批发
医学上,经由尿道插入导尿管到膀胱,引流出尿液。导尿分为导管留置性导尿及间歇性导尿二种。前者导尿管一直留置在病人体内,在病情许可应尽早拔掉管子,须定期更换。后者则每隔4-6小时导尿一次,在膀胱排空后即将导尿管拔出。 注意事项 1.应严格无菌操作,预防尿路感染。 2.插入尿管动作要轻柔,以免损伤尿道粘膜,若插入时有阻挡感可更换方向再插见有尿液流出时再插入2cm,勿过深或过浅,尤忌反复抽动尿管。 3.选择导尿管的粗细要适宜,对小儿或疑有尿道狭窄者,尿管宜细。 4.对膀胱过度充盈者,排尿宜缓慢以免骤然减压引起出血或晕厥。 5.测定残馀尿时,嘱患者先自行排尿,然后导尿。残余尿量一般为5—10ml,如超过100ml,则应留置导尿。 6.留置导尿时,应经常检查尿管情况,有否脱出,必要时以无菌药液每日冲洗膀胱一次;每隔5—7日更换尿管一次,再次插入前应让尿道松弛数小时,再重新插入。

湖南优质导尿回流袋批发
五、拔管方法: 用注射器将气囊中的水抽净,为病人放置好便器,嘱病人自行排尿,尿管可随同尿液一起排出体外,将气囊内液体或气体抽尽后,气囊外部会形成皱壁,拔管时皱擘与尿道黏膜产生摩擦,不同程度地损伤尿道黏膜,病人会有疼痛感,有时出现肉眼血尿,如果抽尽液体或气体后,再次向气囊内推注少量液体或气体(0.4~0.5ml)气囊外部的皱襄消失,气囊平整,拔管时尿管与尿道黏膜不会产生强烈的摩擦,从而减轻尿道损伤,减轻了病人的疼痛。 六、并发症的防治 1、 尿道损伤因护士操作不当,使用气囊尿管致病人尿道损伤,原因有:(1)不了解男性尿道的解剖特点。(2)留置尿管后护理不当,尿袋没固定好,尿袋拉力过大,造成膨大的气囊嵌入尿道。(3)拔管时动作粗暴,气囊内液体未完全抽出强行拔管。 2、拔管困难 拔管困难的原因 (1)气囊导尿管气囊内注入液体过多,气囊回缩不良﹔(2气囊液体过少,形成的球囊小,稍加牵拉或活动水囊向外脱出,压迫尿道、尿道充血、水肿、出血炎症包囊尿管;(3)尿管留置时间过长,尿垢形成附着于气囊外壁;(4)未抽尽气囊内的水或气,而盲目拔管致尿道痉挛。
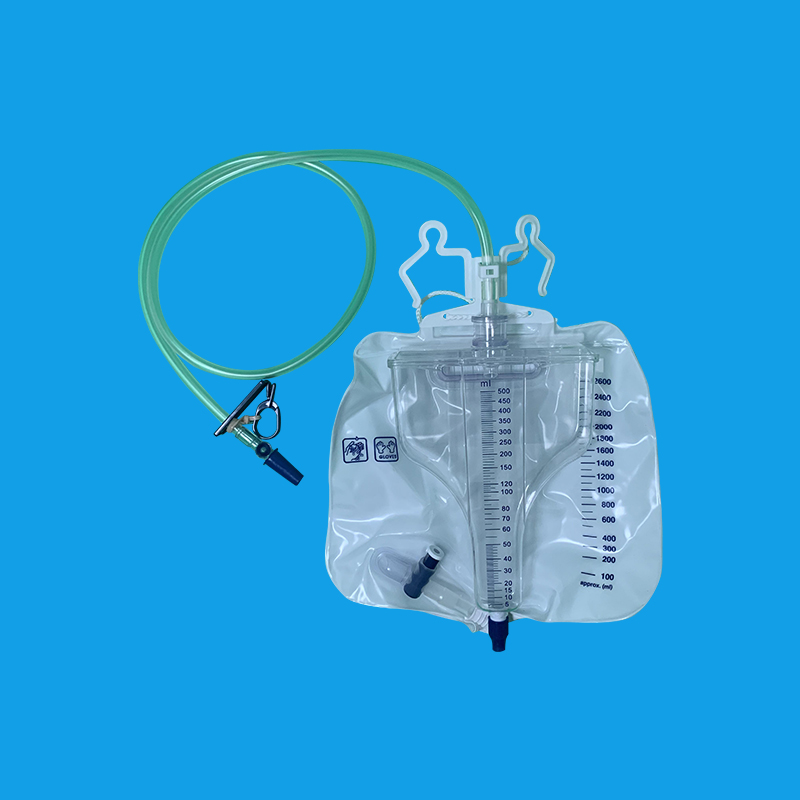
湖南优质导尿回流袋批发
党的十九届五中全会强调坚持创新在我国现代化建设全局中的核心地位,是胸怀两个大局、办好自己的事,育先机、开新局的关键所在。这充分表明以习近平同志为核心的党中央对创新驱动发展战略的高度重视。2021年2月9日,国务院发布第739号令,公布新修订的《医疗器械监督管理条例》(以下简称新《条例》)。新《条例》首次将“保证医疗器械的安全、有效,保障人体健康和生命安全”与“促进医疗器械产业发展”放在并列位置,凸显推动医疗器械产业创新发展的重要性。 本文结合近年来广东省在粤港澳大湾区医疗器械创新发展、医疗器械注册人制度试点及医疗器械审评审批制度改革等方面的工作,阐明新《条例》在鼓励创新方面如何向纵深发展,进一步推动广东省医疗器械产业创新政策落地落实。 一、明确提出推动医疗器械产业高质量发展 医疗器械产业发展,事关人民群众的身体健康和生命安全,事关中华民族健康素质提升和健康中国建设。为加快推进医疗器械产业高质量发展,更好满足人民日益增长的医疗卫生健康需求,提升产业国际竞争力,需要在出台有针对性地引导和扶持政策,加大引进和培养医疗器械专业人才,强化监督管理等方面做好工作。 在产业规划和政策方面,新《条例》提出“将医疗器械创新纳入发展重点”“推动医疗器械产业的高质量发展”,这就要求药品监管部门要主动发挥职能优势和专业优势,更好服务医疗器械产业高质量创新发展。 在完善创新体系方面,新《条例》提出“国家完善医疗器械创新体系,支持医疗器械的基础研究和应用研究,促进医疗器械新技术的推广和应用,在科技立项、融资、信贷、招标采购、医疗保险等方面予以支持。支持企业与高等学校、科研院所、医疗机构等合作开展医疗器械的研究与创新,加强医疗器械知识产权保护,提高医疗器械自主创新能力”。这为医疗器械创新发展提出了方向和办法。 在鼓励激励机制方面,新《条例》提出“对在医疗器械的研究与创新方面做出突出贡献的单位和个人,按照国家有关规定,给予表彰奖励。”这就更能激发单位和个人创新的动力和活力。 广东省药品监管部门将以新《条例》颁布实施为契机,推动出台《广东省推动医疗器械产业高质量发展实施方案》,发挥广东省医疗器械产业既有优势,加强规划引导和政策支持,聚焦重点、突破短板、完善生态,实现产业链整合、价值链提升和市场链优化,力争到2025年,形成一批国内外有影响力的优势特色产品和知名自主品牌的骨干企业,构建产学研用协同联动、稳步发展的医疗器械创新体系,推动医疗器械产业高质量发展,保障和促进公众用械安全。

湖南优质导尿回流袋批发
第四十条 从事医疗器械经营活动,应当有与经营规模和经营范围相适应的经营场所和贮存条件,以及与经营的医疗器械相适应的质量管理制度和质量管理机构或者人员。 第四十一条 从事第二类医疗器械经营的,由经营企业向所在地设区的市级人民政府负责药品监督管理的部门备案并提交符合本条例第四十条规定条件的有关资料。 按照国务院药品监督管理部门的规定,对产品安全性、有效性不受流通过程影响的第二类医疗器械,可以免于经营备案。 第四十二条从事第三类医疗器械经营的,经营企业应当向所在地设区的市级人民政府负责药品监督管理的部门申请经营许可并提交符合本条例第四十条规定条件的有关资料。 受理经营许可申请的负责药品监督管理的部门应当对申请资料进行审查,必要时组织核查,并自受理申请之日起20个工作日内作出决定。对符合规定条件的,准予许可并发给医疗器械经营许可证;对不符合规定条件的,不予许可并书面说明理由。 医疗器械经营许可证有效期为5年。有效期届满需要延续的,依照有关行政许可的法律规定办理延续手续。 第四十三条 医疗器械注册人、备案人经营其注册、备案的医疗器械,无需办理医疗器械经营许可或者备案,但应当符合本条例规定的经营条件。 第四十四条 从事医疗器械经营,应当依照法律法规和国务院药品监督管理部门制定的医疗器械经营质量管理规范的要求,建立健全与所经营医疗器械相适应的质量管理体系并保证其有效运行。 第四十五条 医疗器械经营企业、使用单位应当从具备合法资质的医疗器械注册人、备案人、生产经营企业购进医疗器械。购进医疗器械时,应当查验供货者的资质和医疗器械的合格证明文件,建立进货查验记录制度。从事第二类、第三类医疗器械批发业务以及第三类医疗器械零售业务的经营企业,还应当建立销售记录制度。

湖南优质导尿回流袋批发
原文链接: https://mp.weixin.qq.com/s/NZW-dAANNh8V0NzFQraw0A 近日,备受业内关注的荣研化学株式会社(以下简称荣研化学)与广州迪澳生物科技有限公司(以下简称广州迪澳)专利侵权案件已经有了判决结果。 判决显示:广州迪澳生产销售的“结核分枝杆菌复合群核酸检测试剂盒”涉及两项专利侵权,专利号是:ZL00818262.0和ZL01819083.9,为荣研化学2000年3月28日和2001年9月19日向国家知识产权局提交的名为“合成核酸的方法”和“合成多核苷酸的方法”的发明专利。 北京市磐华律师事务所创始人董巍律师指出,生物检测试剂制品是一类特殊医疗用品,从知识产权保护角度来看,这类案件由于取证和技术比对难度较大,侵权者便将其当做“保护伞”无所顾忌的窃取他人创新成果。但随着民法典施行和国家加快推进专利法修改建立专利侵权惩罚性赔偿制度,以及建立药品专利保护期限补偿制度,对于类似侵权行为会起到强有力的约束作用。 他透露,虽然广州知识产权法院对上述涉及ZL01819083.9专利的案件判令广州迪澳停止制造、许诺销售和销售被诉侵权产品,并在上述两起案件中判令赔偿荣研化学经济损失共计200万元,但这并不意味着案件就此完结。荣研化学会密切关注中国法律条款的变化,不仅是为了挽回自身创新成果受损,也为肃清行业不公平竞争提供范本。 (一)WHO全球示范项目 公开资料显示,荣研化学是拥有80余年历史的日本老牌企业,于1990年1月29日在东京证券交易所第二部上市,并于2002年升格至东京证券交易所一部,主要从事体外诊断试剂盒、医疗器械和基因检测制品的研发、生产、销售,是日本该领域大,也是全球领先的企业之一。 LAMP®(环介导等温扩增)技术是2000年由荣研化学的Notomi博士发明的新型核酸等温扩增技术。TB-LAMP结核分枝杆菌复合群核酸快速诊断系统由盖茨基金赞助,荣研化学与FIND基金共同研制。自2012年起,世界卫生组织(WHO)评估了17个国家20项研究。2016年1月份,WHO指南编写组召开会议并推荐了TB-LAMP。 Notomi博士在接受媒体采访时表示,一般的核酸扩增法需要2.5~5小时的反应时间,而“Loopamp®结核分枝杆菌复合群核酸检测试剂盒”只需要约1小时就能得出结果,TB-LAMP更使用了“Loopamp®PURE DNA提取或纯化试剂试剂盒”成功缩短了DNA的提取时间。另外,样本种类除了咳痰以外,支气管洗净液、胃液、胸水等也能使用。 据了解,北京蓝谱生物科技有限公司(以下简称“蓝谱生物”) 是荣研化学在中国(包括港澳)地区重要的合作伙伴。北京蓝谱生物科技有限公司总经理李奉京透露,2010-2012年间,蓝谱生物与广州迪澳都是荣研化学的合作伙伴。 2012年,蓝谱生物与广州迪澳解除合作协议。2013年,广州迪澳“结核分枝杆菌复合群核酸检测试剂盒”获批,注册证编号为国食药监械(准)字2013第3402079号,管理类别为“第三类”。2019年该企业提交产品注销申请,同时再次提交产品注册申请,2019年5月拿到新注册证,编号为国械注准20193400313。