福州优质导尿回流袋厂家
发布时间:2022-03-29 00:41:50
福州优质导尿回流袋厂家
近日,广东省医保局发布《关于广东省十三届人大四次会议第1116号代表建议协办意见的函》 意见函针对强医疗器械行业自主研发能力,保障全民健康水平的建议做出了回复。 一、建立医保支付标准和集中采购协同机制 支持国产医用耗材行业发展 建立健全医保支付标准与医用耗材集中采购协同机制,通过制定医用耗材集中采购中选品种和非中选品种的医保支付标准,支持国产优质医用耗材研发和使用,促进国产医用耗材行业发展。 2020年12月,广东省印发《关于贯彻落实<国家医疗保障局关于国家组织冠脉支架集中带量采购和使用配套措施使的意见>的通知》(粤医保发〔2020〕42号),要求各地级以上市医保部门做好冠脉支架医保支付标准制订工作。国家组织冠脉支架集中采购中选品种的中选价作为支付标准,全额纳入医保基金支付范围,对非中选品种设定高医保支付标准,并结合当地实际,采取相应措施,两年内逐步调整支付标准,使其不超过高中选价。 各地级以上市医保局通过制定国家组织冠脉支架集中带量采购中选品种的支付标准,规范相应医用耗材的医保支付工作,鼓励医疗机构优先使用国家集中采购中选的国产医用耗材。 二、将符合条件的医用耗材纳入医保支付范围 2021年3月,我省印发《广东省基本医疗保险、工伤保险和生育保险医用耗材目录(2021年)》(粤医保发〔2021〕14号),将临床价值高、经济性评价优良的医用耗材纳入医保支付范围,进一步明确了医用耗材的医保支付范围,参保人按规定使用目录内的医用耗材时,医保基金按规定支付,减轻了参保人医疗费用负担,同时促进了国产医用耗材产业发展。 三、完善招标采购机制支持国产耗材的研发和使用 促进国产耗材的替代 一是出台《广东省医疗保障局关于做好药品和医用耗材采购工作的指导意见》(粤医保规〔2020〕2号),要求全省各级公立医疗机构使用的药品和医用耗材统一在采购平台上采购,凡已取得国家药监部门颁发的正式生产批件的产品均可选择在省平台、广州平台、深圳平台报名挂网交易,医疗机构按临床需要在网上采购使,用逐步实现“挂网交易、全省可采”,降低企业销售成本。 对于采购平台上无企业挂网的短缺品种、应对公共卫生突发事件的应急审批或紧急紧缺品种、未发生实际交易或其他原因导致采购困难且临床必需、临床使用量极少等类型的医用耗材,医疗机构可在年度采购总金额5%范围内自主议价采购,促进国产医用耗材尽快投入临床使用。二是在制定我省医用耗材集采规则中,实行国产医用耗材和进口医用耗材同类同组竞价政策,提升国产医用耗材的价格优势,增加国产医用耗材中选几率。
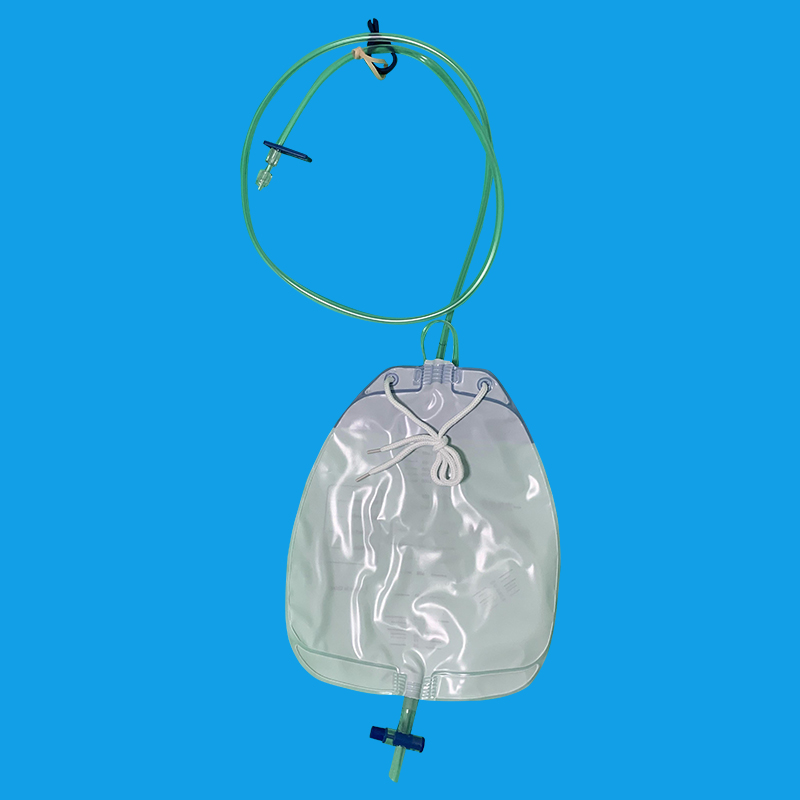
福州优质导尿回流袋厂家
。 在中国,做类似手术器械和耗材的公司不少,但是能够在高端领域拥有市场地位的并不多。 乐普医疗(3000003),便是其中有冠军相的龙头之一。 在另一篇分析信立泰的文章《从广东省委到百亿富豪,他的前半生是李达康,后半生却成了王大路》的文章中,我们讲过—— 心血管疾病,是全世界夺去人类生命的一大疾病。 根据世界卫生组织的统计,2012年有1750万人死于心血管疾病,其中冠心病占到了42%。 冠心病,通常是由于人老了之后,血管里含有胆固醇的渣滓越来越多,后堵塞住了血管,让血液无法流动,严重的就会导致胸疼、气喘、疲劳及心脏病等症状。 治疗这种疾病的常见办法是“支架植入手术”, 简单来说,就是放一个支架进血管里,把它撑起来,让狭窄的部分重新扩大,保持血流通畅。

福州优质导尿回流袋厂家
三、明确支持创新医疗器械临床推广和使用 新《条例》明确了可以免于进行临床评价的情形和临床评价的要求,新增了国家支持医疗机构开展临床试验,鼓励医疗机构开展创新医疗器械临床试验,新增了安全性数据可以用于医疗器械注册申请的情形。这些规定进一步优化了临床评价和临床试验要求,有助于支持创新产品临床推广和使用。 新《条例》规定了医疗机构因临床急需进口少量医疗器械的,经国务院药品监督管理部门或者国务院授权的省、自治区、直辖市人民政府批准,可以进口。进口的医疗器械应当在指定医疗机构内用于特定医疗目的。鼓励在国际具有临床应用先进性的、在国内尚未上市医疗器械,在指定医疗机构先行先试。 广东省药品监管部门将以新《条例》颁布实施为契机,贯彻落实好国家市场监管总局等八部门联合发布的《粤港澳大湾区药品医疗器械监管创新发展工作方案》,允许临床急需、港澳公立医院已采购使用、具有临床应用先进性的医疗器械,通过香港大学深圳医院试点,发现问题、理清思路、找到办法,进而把实践经验固化到配套制度之中,为政策在粤港澳大湾区全面实施奠定制度保障基础。同时,将内地药品监管体制与港澳监管体制进行有效对接,进一步完善粤港澳药品监管制度衔接机制,促进我国药品监管体系和监管能力现代化水平的整体提升,为保障人民群众用药用械安全提供宝贵经验。
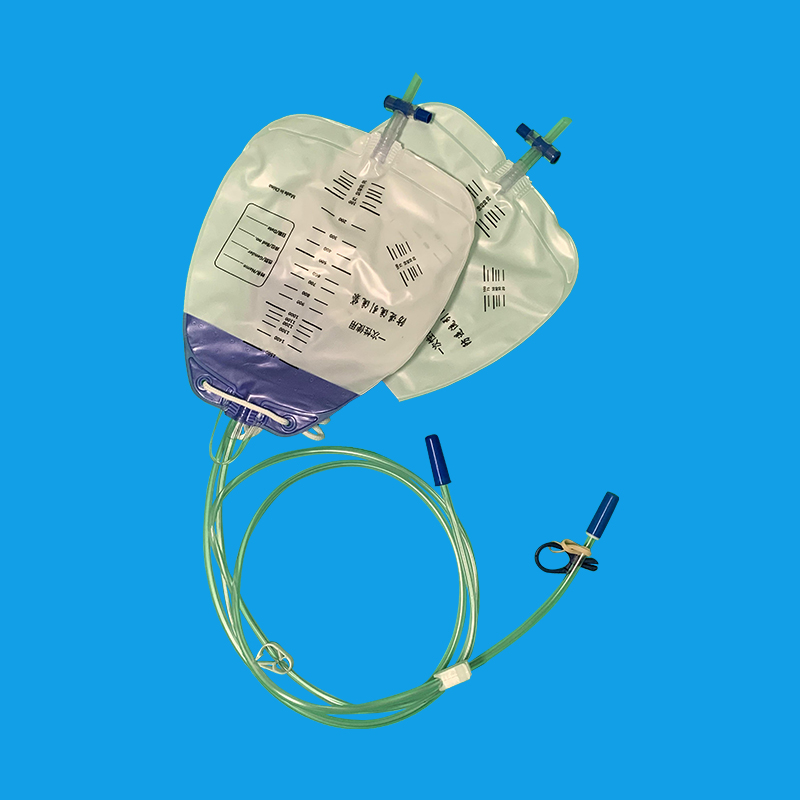
福州优质导尿回流袋厂家
MDx组委: 您和团队在新冠疫情中也有非常多的工作与成果,那么也请您谈谈对于变异株频繁发现等全球疫情背景下,您对于新冠病毒检测的新思考?接下来应当引起注意的有哪些关键点?对于新冠疫苗,中和抗体检测方面您有哪些建议想法? 李教授: 变异株频现的背景下,新冠病毒检测试剂首先要自证清白,主要是漏检问题,包括灵敏度降低甚至假阴性问题,无论核酸检测还是抗原检测都需要拿出数据,无论真实世界数据还是模拟临床数据。新冠同多数疾病一样,会呈现出多种检测系统共存的局面,孰优孰劣,往往不是技术说了算,而是市场说了算。 疫苗接种后,需要关注的是抗原性漂移(drift)和转移(shift)问题,二者分属量变到质变不同阶段,但都需要密切监测变异的发生和累积,变异检测要常规开展起来。实际上,目前也是这么做的,但仅仅测序不够,还需要更高密度的人群监测,这需要快速检测试剂,尤其是针对那些值得警惕的变异(variant of concern, VOC)和值得关注的变异(variant of interest, VOI)。可以预期,VOC和VOI的名单会不断变化,需要人们快速行动,及时推出针对性的快速检测体系来。 MDx组委: 您在核酸检测,多重核酸分析等方向均有丰富的研究及转化成果,那么对于在新冠刺激下目前行业内风头正起的病原多重联合检测技术,想听听您的看法和评价如何,尤其是在结核等传染病的分子诊断方面,对于行业有什么建议? 李教授: 相对于新冠病毒而言,结核等其它传染病的分子诊断更为复杂:比如,多病原体联合检测就面临检测平台、临床试验和临床意义等多方面挑战。 就结核而言,分枝杆菌是一大类病原体,感染症状相似,但治疗手段差别很大,需要甄别出结核分枝杆菌和非结核分枝杆菌的具体种类,本身就极具挑战性。目前,我国结核分枝杆菌核酸筛查普及率不够高,一个特殊原因是合适的样本类型还未得到很好的解决。再有就是耐药突变的发生,这是结核治疗的老大难问题,耐药检测不充分,和治疗不充分一样,会导致大量问题的发生。 我国对于新冠确实控制得很好,目前是新冠肺炎低负担国家,然而不幸的是,我国一直都是结核病高负担国家,和印度、印尼等发展中国家一起名列前茅。原因固然很多,但与总体投入偏少不无关系。分子诊断行业固然需要继续努力,持续研发质优价廉的诊断产品,但疾病本身的防控也需要全社会的高度重视。 MDx组委: 您作为厦大分子诊断教育部工程研究中心主任以及致善生物董事长,也想请您简单谈谈,接下来在后疫情时代,您和厦大团队在分子诊断领域的研究计划,以及关于致善在分子诊断领域的布局有哪些思考? 李教授: 我们这个团队的底色决定了它的研究型和创新型特质。一方面,我们将继续深耕多靶标熔解曲线技术这一优势技术领域,通过持续的研发投入和技术创新,力争解决一些相对复杂的分子诊断难题;另一方面,也将围绕分子诊断的关键问题,通过多种形式的合作,努力打造良性的生态系统,形成多方共赢的局面。 MDx组委:感谢李教授的精彩分享!敬请期待李教授在会议现场带来更多专业分享!