河南优质女士集尿袋厂家
发布时间:2022-06-24 00:41:28
河南优质女士集尿袋厂家
医疗器械是与人类生命健康息息相关的产品,世界各国对医疗器械行业的发展高度重视。近年来随着我国经济发展“供给侧结构性改革”战略的实施,将医疗器械产业的发展列入了国家发展战略中,医疗器械行业进入高速发展期,逐渐跻身国际医疗器械行业,从消费大国逐渐转化为制造大国和出口大国。 随着全球公众健康意识增强,医疗服务机构对高品质医疗器械的要求不断提高,各国政府为提升医疗器械的安全性制定了相应的法律法规,以保护民众的生命安全。 因此我国医疗器械行业在走出国门时有必要对相关国家的法律法规有所了解,并知晓相应的监管要求和市场需求的方向,针对性地采取相应的策略和措施,稳步推进,不断提高产品的能级,逐步扩大海外市场。本期小编整理了中国主要出口国家和地区医疗器械的准入要求,供大家参考。 1、医疗器械定义 医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件。 2.常见医疗器械产品海关税则号与名称 3、主要国家和地区分类及要求 美国FDA 美国食品药品监督管理局(简称:FDA),其职责是确保美国本国生产或进口的食品、化妆品、药物、生物制剂、医疗设备和放射产品等的安全,同时也负责执行公共卫生条件及州际旅行和运输的检查、对于诸多产品中可能存在的疾病的控制等。 分类 医疗器械范围很广,小到医用手套,大至心脏起博器,均在FDA监督之下,根据医疗用途和对人体可能的伤害,FDA将医疗器械分为Ⅰ、Ⅱ、Ⅲ类,等级越高监督越严。 一类(低至中度风险):普通管理。是指风险小或无风险的产品。 第二类(中度至高度风险):普通+特殊管理。其管理是在“普通管理”的基础上,还要通过实施标准管理或特殊管理,以保证质量和安全有效性。 第三类(高风险):上市前批准管理(PMA)。是指具有较高风险或危害性,或是支持或维护生命的产品,例如人工心脏瓣膜、心脏起搏器、人工晶体、人工血管等。 准入要求 对Ⅰ类产品,企业向FDA递交相关资料并审核通过后,FDA只进行公告,但并无相关证件发给企业; 对Ⅱ、Ⅲ类器械,企业须递交PMN或PMA,FDA在公告的同时,会给企业以正式的市场准入批准函件(Clearance),即允许企业以自己的名义在美国医疗器械市场上直接销售其产品。至于申请过程中是否到企业进行现场GMP考核,则由FDA根据产品风险等级、管理要求和市场反馈等综合因素决定。

河南优质女士集尿袋厂家
留置导尿管在临床上是很常见的一种操作,留置导尿管不仅可以缓解急性尿潴留病人腹部胀痛的情况,同时对于全麻手术的病人,通常也在术前需要留置导尿管。以男性病人为例,简单介绍留置导尿管的过程,首先患者要采取平卧位,操作前要对男性龟头以及尿道口进行充分消毒,消毒完毕以后铺无菌的操作单。其次打开无菌导尿包,用石蜡油将尿管润滑,左手将男性的阴茎拎起,右手用镊子夹住导尿管远端,插入男性尿道口,在插入的过程中要缓慢,避免对尿道黏膜造成损伤,看到尿液从尿管中流出时说明已经插入膀胱,用注射器打上球囊,就可以固定导尿管,导尿管远端接上引流袋就可以了。

河南优质女士集尿袋厂家
2020年9月14日,对中国冠心病患者而言是个好日子。 在高值耗材国家性集采的启动会议上,医保局确认,冠脉支架将成为首批实施全国集采的耗材品种。 与药品市场相同,集中采购意味着企业将在竞争中进行低价厮杀,“以价换量”。从此前江苏省试点集采的结果来看,冠脉支架的平均降价幅度为51%,高可达到66.1%。因此,如无意外,明年1月份冠脉支架在大型公立医院的售价将会“腰斩”。 冠心病患者所用到的支架,到底是个啥? 冠心病,或称缺血性心脏病,是世界人口的头号杀手之一。它是由于冠状动脉血管发生病变而引起血管腔狭窄或阻塞的心脏病,临床表现包括心绞痛、心肌梗死等,有1/3患者临床症状为猝死。 冠心病有效的治疗方式是PCI(经皮冠状动脉介入)手术。小巧而精细的冠脉支架,是这一手术中为关键的耗材。PCI手术的基本原理,就是将支架植入冠状动脉血管,将动脉壁撑开,使血流恢复通畅。 一台PCI手术的费用大约在2.5-3.5万元,其中冠脉支架的价格就占到一半。国产支架价格在8000~11000元,进口支架还要翻一番,高达到23000元。因此,如果冠脉支架的价格能够减半,对于患者而言无疑是极大的减负。 但是,昂贵的高值耗材并不止冠脉支架一种。为什么冠脉支架会成为全国性耗材集采的“先驱”呢? 这个问题的答案隐含着医疗器械行业关键的一个逻辑:国产替代。 因为心血管是我国一大疾病,利润高也吸引到了很多本土玩家前赴后继。其实,从进口支架漫天要价的2011年以来,到如今国产支架的市场份额已经超过75%,乐普医疗、微创医疗、吉威医疗和赛诺医疗四家头部企业占据了大部分市场,且比例相当稳定。 但与之相对的是,像神经介入器械、手术机器人、人工关节等高精尖领域的专科耗材,国产和进口的比例几乎倒置;而除了耗材之外,高端医疗设备领域也由外企垄断,80%的CT市场、90%的超声波仪器市场、90%的磁共振设备均为国外品牌所占据。 高性能核磁共振成像系统、高端CT机价格通常在500万元以上,而高性能的设备意味着更清晰的图像,在肿瘤等疾病诊断上面,高一个清晰度意味着能看到更详细的人体组织信息。几十个像素点的差距,就能影响医生对疾病的诊断。 如果病人明明有瘤块,却未显示在图像中,那这多花几百块钱做的检测起到的就完全是负作用。所以国产的虽然有价格优势,但是对于大医院和病人来讲,在疾病面前有些钱省不得,而这些高端影像器械长期垄断在“GPS”(通用电气、飞利浦、西门子)三大厂家。 之所以国产化率不同,是因为各种产品所处的发展阶段不同。
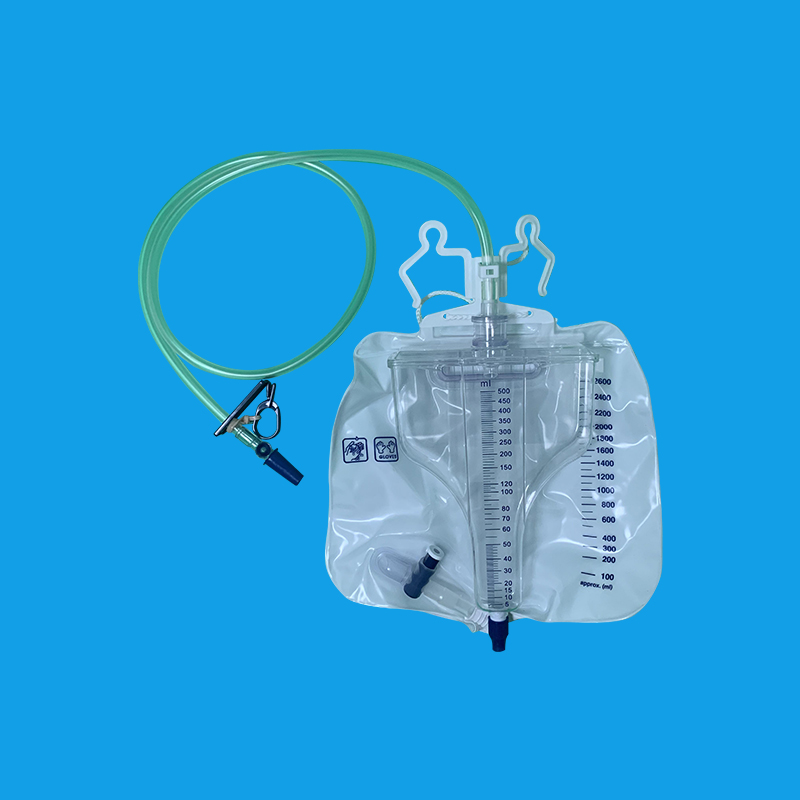
河南优质女士集尿袋厂家
三、明确支持创新医疗器械临床推广和使用 新《条例》明确了可以免于进行临床评价的情形和临床评价的要求,新增了国家支持医疗机构开展临床试验,鼓励医疗机构开展创新医疗器械临床试验,新增了安全性数据可以用于医疗器械注册申请的情形。这些规定进一步优化了临床评价和临床试验要求,有助于支持创新产品临床推广和使用。 新《条例》规定了医疗机构因临床急需进口少量医疗器械的,经国务院药品监督管理部门或者国务院授权的省、自治区、直辖市人民政府批准,可以进口。进口的医疗器械应当在指定医疗机构内用于特定医疗目的。鼓励在国际具有临床应用先进性的、在国内尚未上市医疗器械,在指定医疗机构先行先试。 广东省药品监管部门将以新《条例》颁布实施为契机,贯彻落实好国家市场监管总局等八部门联合发布的《粤港澳大湾区药品医疗器械监管创新发展工作方案》,允许临床急需、港澳公立医院已采购使用、具有临床应用先进性的医疗器械,通过香港大学深圳医院试点,发现问题、理清思路、找到办法,进而把实践经验固化到配套制度之中,为政策在粤港澳大湾区全面实施奠定制度保障基础。同时,将内地药品监管体制与港澳监管体制进行有效对接,进一步完善粤港澳药品监管制度衔接机制,促进我国药品监管体系和监管能力现代化水平的整体提升,为保障人民群众用药用械安全提供宝贵经验。